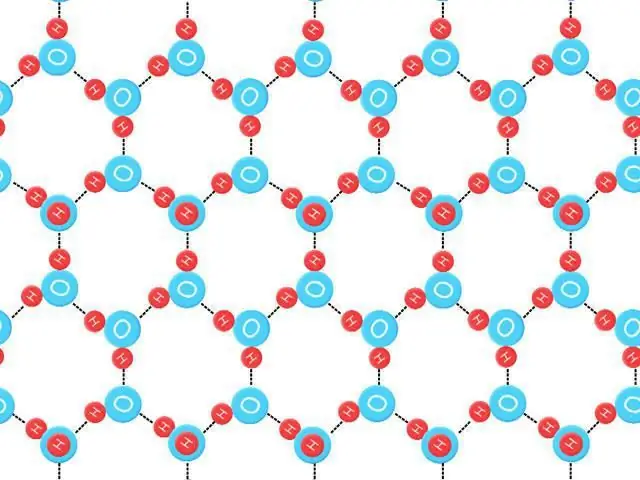
Сұйық судың үш өлшемді күйін зерттеу қиын, бірақ мұз кристалдарының құрылымын талдау арқылы көп нәрсе білді. Төрт көршілес сутегімен әрекеттесетін оттегі атомдары тетраэдрдің төбелерін алып жатыр (тетра=төрт, хедрон=жазықтық). Мұздағы мұндай байланысты үзу үшін қажетті орташа энергия 23 кДж/моль-1 деп есептеледі.

Су молекулаларының сутегі тізбегінің берілген санын, сондай-ақ берілген күшті құра алу қабілеті әдеттен тыс жоғары балқу температурасын тудырады. Ол еріген кезде оны құрылымы біркелкі емес сұйық су ұстайды. Сутегі байланыстарының көпшілігі бұзылған. Сутегімен байланысқан мұздың кристалдық торын бұзу үшін жылу түрінде көп энергия қажет.
Мұздың пайда болу ерекшеліктері (Ih)
Тұрғындардың көпшілігі кристалдық торлы мұздың қандай түрі бар деп қызық. ҚажеттіАйта кету керек, көптеген заттардың тығыздығы мұздату кезінде, молекулалық қозғалыстар баяулағанда және тығыз орналасқан кристалдар пайда болған кезде артады. Судың тығыздығы максимум 4°C (277K) температурада салқындаған сайын артады. Содан кейін температура осы мәннен төмен түссе, ол кеңейеді.
Бұл өсу торы мен тығыздығы төмен сутегімен байланысқан ашық мұз кристалының түзілуіне байланысты, онда әрбір су молекуласы жоғарыдағы элементпен және басқа төрт мәнмен қатаң байланысқан, сонымен бірге жеткілікті жылдам қозғалады. массасы көбірек. Бұл әрекет орын алғандықтан, сұйықтық жоғарыдан төменге қарай қатып қалады. Мұның маңызды биологиялық нәтижелері бар, нәтижесінде тоғандағы мұз қабаты тірі жандарды қатты суықтан оқшаулайды. Сонымен қатар, судың екі қосымша қасиеті оның сутегі сипаттамаларына байланысты: меншікті жылу және булану.
Құрылымдардың толық сипаттамасы
Бірінші критерий - заттың 1 грамм температурасын 1°C-қа көтеру үшін қажетті мөлшер. Судың дәрежесін көтеру салыстырмалы түрде үлкен жылуды қажет етеді, өйткені әрбір молекула кинетикалық энергияның жоғарылауы үшін үзілуі керек көптеген сутектік байланыстарға қатысады. Айтпақшы, H2O-ның барлық ірі көпжасушалы организмдердің жасушалары мен ұлпаларында көп болуы жасушалар ішіндегі температура ауытқуларының барынша азайғанын білдіреді. Бұл қасиет өте маңызды, өйткені биохимиялық реакциялардың көпшілігінің жылдамдығысезімтал.
Судың булану жылуы да көптеген басқа сұйықтықтарға қарағанда айтарлықтай жоғары. Бұл денені газға айналдыру үшін көп мөлшерде жылу қажет, өйткені су молекулалары бір-бірінен ажырап, аталған фазаға өтуі үшін сутектік байланыстар үзілуі керек. Өзгермелі денелер тұрақты дипольдер болып табылады және басқа ұқсас қосылыстармен және иондайтын және ерітетін қосылыстармен әрекеттесе алады.
Жоғарыда аталған басқа заттар полярлық болған жағдайда ғана жанасуы мүмкін. Бұл элементтердің құрылымына дәл осы қосылыс қатысады. Сонымен қатар, ол су молекулаларының оттегінің теріс атомдары катиондарға, ал оң иондар мен сутегі атомдары аниондарға бағытталған етіп электролиттерден түзілген осы бөлшектердің айналасында туралай алады.
Қатты денелерде, әдетте, молекулалық кристалдық торлар және атомдық торлар түзіледі. Яғни, йод құрамында I2, болатындай етіп салынса, қатты көмірқышқыл газында, яғни құрғақ мұзда CO2 молекулалары болады. кристалдық тор түйіндерінде орналасқан. Ұқсас заттармен әрекеттесу кезінде мұзда иондық кристалдық тор болады. Мысалы, көміртегіге негізделген атомдық құрылымы бар графит оны алмас сияқты өзгерте алмайды.
Ас тұзының кристалы суда ерігенде не болады: полярлы молекулалар кристалдағы зарядталған элементтерге тартылады, бұл оның бетінде натрий мен хлоридтің ұқсас бөлшектерінің түзілуіне әкеледі, нәтижесінде осы денелер пайда боладыбір-бірінен ажырайды және ол ери бастайды. Осы жерден мұздың иондық байланысы бар кристалдық торы бар екенін байқауға болады. Әрбір еріген Na+ бірнеше су молекуласының теріс ұштарын тартады, ал әрбір еріген Cl - оң ұштарын тартады. Әрбір ионды қоршап тұрған қабық шығу сферасы деп аталады және әдетте еріткіш бөлшектерінің бірнеше қабатынан тұрады.
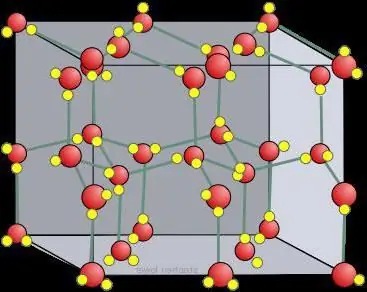
Құрғақ мұз кристалды торы
Айнымалылар немесе элементтермен қоршалған ион сульфатталған деп аталады. Еріткіш су болған кезде мұндай бөлшектер гидратталған. Осылайша, кез келген полярлы молекула сұйық дененің элементтерімен ерітуге бейім. Құрғақ мұзда кристалдық тордың түрі агрегаттық күйдегі атомдық байланыстарды түзеді, олар өзгермейді. Тағы бір нәрсе - кристалды мұз (мұздатылған су). Карбоксилаза және протондалған аминдер сияқты иондық органикалық қосылыстар гидроксил және карбонил топтарында еритін болуы керек. Мұндай құрылымдардың құрамындағы бөлшектер молекулалар арасында қозғалады және олардың полярлық жүйелері осы денемен сутектік байланыстар түзеді.
Әрине, молекуладағы соңғы көрсетілген топтардың саны оның ерігіштігіне әсер етеді, бұл элементтегі әртүрлі құрылымдардың реакциясына да байланысты: мысалы, бір, екі және үш көміртекті спирттер араласады. сумен, бірақ бір гидроксил қосылыстары бар үлкенірек көмірсутектер сұйықтықтарда әлдеқайда аз сұйылтылған.
Алтыбұрышты Ih пішіні бойынша ұқсасатомдық кристалдық тор. Мұз және жердегі барлық табиғи қар үшін бұл дәл осылай көрінеді. Бұған су буынан (яғни қар түйіршіктерінен) өскен мұздың кристалдық торының симметриясы дәлел. Ол 194-тен Р 63/мм ғарыш тобында; D 6h, Laue класы 6/мм; β-ға ұқсас, оның еселігі 6 бұрандалы ось бар (оның бойымен ығысудан басқа айнала айналу). Оның қарапайым текше (~1/2) немесе бет центрленген текше (~3/4) құрылымдармен салыстырғанда тиімділігі төмен (~1/3) болатын жеткілікті ашық төмен тығыздық құрылымы бар.
Қарапайым мұзбен салыстырғанда, CO2 молекулаларымен байланысқан құрғақ мұздың кристалдық торы статикалық болып табылады және атомдар ыдырағанда ғана өзгереді.
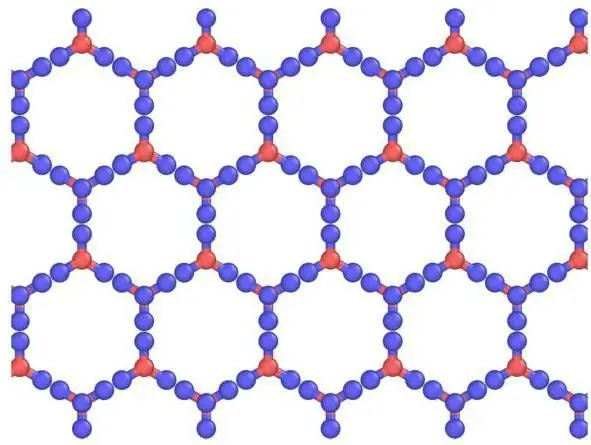
Торларды және олардың элементтерін сипаттау
Кристаллдарды бірінің үстіне бірі орналасқан парақтардан тұратын кристалды үлгілер ретінде қарауға болады. Сутегі байланысы реттелген, ал шын мәнінде бұл кездейсоқ, өйткені протондар шамамен 5 К жоғары температурада су (мұз) молекулалары арасында қозғала алады. Шынында да, протондар тұрақты туннельдік ағында кванттық сұйықтық сияқты әрекет етуі мүмкін. Бұл нейтрондардың шашырауымен күшейтіліп, олардың шашырау тығыздығын оттегі атомдары арасындағы жарты жолда көрсетіп, локализация мен үйлесімді қозғалысты көрсетеді. Мұнда мұздың атомдық, молекулалық кристалдық торға ұқсастығы бар.
Молекулаларда сутегі тізбегі сатылы орналасадыұшақтағы үш көршісіне қатысты. Төртінші элементте тұтылған сутегі байланысының орналасуы бар. Мінсіз алтыбұрышты симметриядан шамалы ауытқу бар, өйткені бірлік ұяшық осы тізбектің бағытында 0,3% қысқа. Барлық молекулалар бірдей молекулалық ортаны бастан кешіреді. Әрбір «қораптың» ішінде интерстициалды судың бөлшектерін ұстау үшін жеткілікті орын бар. Жалпы қарастырылмаса да, олар жақында мұздың ұнтақты кристалдық торының нейтрондық дифракциясы арқылы тиімді түрде анықталды.
Заттарды өзгерту
Алтыбұрышты дененің сұйық және газ тәрізді сумен 0,01 ° C, 612 Па, қатты элементтермен үш еселік нүктелері бар - үш -21,985 ° C, 209,9 МПа, он бір және екі -199,8 ° C, 70 МПа, сонымен қатар - 34,7 ° C, 212,9 МПа. Алтыбұрышты мұздың диэлектрлік өтімділігі 97,5.
Бұл элементтің балқу қисығы МПа арқылы берілген. Күй теңдеулері, оларға қосымша, физикалық қасиеттердің өзгеруіне алтыбұрышты мұздың және оның сулы суспензияларының температурасына қатысты кейбір қарапайым теңсіздіктер бар. Қаттылық 0°C температурада гипстен (≦2) төмен немесе -80°C температурада дала шпатына (6 Мох) дейін көтеріледі, бұл абсолютті қаттылықтың әдеттен тыс үлкен өзгерісі (> 24 есе).
Мұздың алтыбұрышты кристалдық торы алтыбұрышты тақталар мен бағандарды құрайды, олардың жоғарғы және төменгі беттері 5,57 мкДж см энтальпиясы бар {0 0 0 1} базальды жазықтықтар -2және басқа эквивалентті бүйір бөліктері 5, 94 болатын {1 0 -1 0} призманың бөліктері деп аталады.µДж см -2. 6,90 ΜДж ˣ см -2 болатын қосалқы беттерді {1 1 -2 0} құрылымдардың бүйірлері түзетін жазықтықтар бойымен қалыптастыруға болады.
Мұндай құрылым қысымның жоғарылауымен жылу өткізгіштіктің аномальді төмендеуін көрсетеді (сонымен қатар тығыздығы төмен текше және аморфты мұз), бірақ көптеген кристалдардан ерекшеленеді. Бұл мұз бен судың кристалдық торындағы дыбыстың көлденең жылдамдығын төмендететін сутегі байланысының өзгеруіне байланысты.
Үлкен кристалды үлгілерді және кез келген қалаған мұз бетін қалай дайындау керектігін сипаттайтын әдістер бар. Зерттелетін алтыбұрышты дененің бетіндегі сутектік байланыс көлемдік жүйенің ішіне қарағанда реттелген болады деп болжанады. Фазалық-торлы жиілікті генерациялайтын вариациялық спектроскопия алтыбұрышты мұздың базальды бетінің жер асты HO тізбегіндегі екі жоғарғы қабат (L1 және L2) арасында құрылымдық ассиметрия бар екенін көрсетті. Алтыбұрыштардың жоғарғы қабаттарындағы қабылданған сутектік байланыстар (L1 O ··· HO L2) екінші қабатта жоғарғы жинақтауға (L1 OH ··· O L2) қабылданғанға қарағанда күштірек. Интерактивті алтыбұрышты мұз құрылымдары қолжетімді.
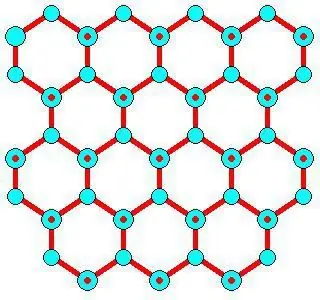
Әзірлеу мүмкіндіктері
Мұзды қалыптастыру үшін қажетті су молекулаларының ең аз саны шамамен 275 ± 25, 280 толық икосаэдрлік кластер сияқты. Түзу 10 жылдамдықпен жүреді 10 ауа-су интерфейсі және сусымалы суда емес. Мұз кристалдарының өсуі әртүрлі өсу қарқынына байланыстыэнергиялар. Биологиялық үлгілерді, тағамды және мүшелерді криоконсервациялау кезінде суды қатып қалудан қорғау керек.
Бұған әдетте шағын үлгілерді және криоконсерваторды пайдалану арқылы жылдам салқындату жылдамдығы және мұзды ядролау және жасуша зақымдануын болдырмау үшін қысымды арттыру арқылы қол жеткізіледі. Мұздың/сұйықтықтың бос энергиясы атмосфералық қысымда ~30 мДж/м2-тан 200 МПа-да 40 мДж/м-2 дейін артады. бұл әсердің пайда болу себебі.
Мұзға кристалдық тордың қандай түрі тән
Балама ретінде олар призма беттерінен (S2), тез қатқан немесе шайқалған көлдердің кездейсоқ бұзылған бетінде тезірек өсе алады. {1 1 -2 0} беттерінен өсу кем дегенде бірдей, бірақ оларды призмалық негіздерге айналдырады. Мұз кристалының дамуы туралы деректер толығымен зерттелді. Әртүрлі беттердің элементтерінің салыстырмалы өсу қарқыны буындарды ылғалдандырудың үлкен дәрежесін қалыптастыру мүмкіндігіне байланысты. Айналадағы судың температурасы (төменгі) мұз кристалындағы тармақталу дәрежесін анықтайды. Бөлшектердің өсуі өте салқындаудың төмен дәрежесінде диффузия жылдамдығымен шектеледі, яғни <2 ° C, нәтижесінде олардың саны артады.

Бірақ >4°C депрессияның жоғары деңгейлерінде даму кинетикасымен шектелген, нәтижесінде ине өседі. Бұл пішін құрғақ мұздың құрылымына ұқсас (алты қырлы құрылымы бар кристалдық торы бар), әртүрлібетінің даму сипаттамалары және қар бүршіктерінің жалпақ пішіндерінің артындағы қоршаған (өте суыған) судың температурасы.
Атмосферада мұздың пайда болуы бұлттардың пайда болуына және қасиеттеріне қатты әсер етеді. Жылына миллиондаған тонна атмосфераға түсетін шөл шаңында кездесетін дала шпаттары маңызды түзуші болып табылады. Компьютерлік модельдеу мұның жоғары энергиялы беттік жазықтықтардағы призмалық мұз кристалдық жазықтықтарының ядролануына байланысты екенін көрсетті.
Кейбір басқа элементтер мен торлар
Ерітілген заттар (өте ұсақ гелий мен сутекті қоспағанда, олар аралықтарға түсе алады) атмосфералық қысымда Ih құрылымына кіре алмайды, бірақ олардың бөлшектері арасындағы бетке немесе аморфты қабатқа күштеп шығарылады. микрокристалды дене. Құрғақ мұздың торлы орындарында басқа да элементтер бар: NH4 + және Cl - сияқты хаотропты иондар, олар Na + және SO42-сияқты басқа космотроптыларға қарағанда жеңілірек сұйық мұздатуға кіреді, сондықтан оларды жою мүмкін емес, себебі олар кристалдар арасында қалған сұйықтықтың жұқа қабығын құрайды. Бұл қалған зарядтарды теңестіретін (бұл магниттік сәулеленуге де әкелуі мүмкін) беткі судың диссоциациясына және қалдық сұйық қабықшалардың рН өзгеруіне байланысты беттің электрлік зарядталуына әкелуі мүмкін, мысалы, NH 42SO4 қышқылдырақ және NaCl негізді болады.
Олар беттерге перпендикулярмұздың кристалдық торы бекітілген келесі қабат (қара түспен O атомдары бар). Олар баяу өсетін {0 0 0 1} базальды бетімен сипатталады, мұнда тек оқшауланған су молекулалары бекітіледі. Жаңадан қосылған бөлшектер жұптары бір-бірімен сутекпен (бір сутегі байланысы/элементтің екі молекуласы) байланыса алатын призманың жылдам өсетін {1 0 -1 0} беті. Ең жылдам өсетін бет {1 1 -2 0} (екінші призмалық), мұнда жаңадан қосылған бөлшектердің тізбектері бір-бірімен сутектік байланыс арқылы әрекеттесе алады. Оның тізбегінің/элемент молекуласының бірі - призманың екі жағына айналуын ынталандыратын және бөлетін жоталарды құрайтын пішін.
Нөлдік энтропия
S 0=k B ˣ Ln (N E0) ретінде анықтауға болады, мұндағы k B - Больцман тұрақтысы, NE E энергиясындағы конфигурациялар саны, ал E0 - ең төменгі энергия. Кельвин нөліндегі алтыбұрышты мұз энтропиясының бұл мәні термодинамиканың үшінші заңын бұзбайды «Идеал кристалдың абсолютті нөлдегі энтропиясы дәл нөлге тең», өйткені бұл элементтер мен бөлшектер идеалды емес, сутектік байланысы ретсіз.
Бұл денеде сутегі байланысы кездейсоқ және тез өзгереді. Бұл құрылымдар энергия бойынша дәл бірдей емес, бірақ энергетикалық жақын күйлердің өте үлкен санына таралады, «мұз ережелеріне» бағынады. Нөлдік энтропия - бұл материалды абсолютті салқындату мүмкін болса да сақталатын бұзылыснөл (0 K=-273, 15 ° C). Алтыбұрышты мұз 3, 41 (± 0, 2) ˣ моль -1 ˣ K -1 үшін тәжірибелік шатасуды тудырады. Теориялық тұрғыдан белгілі мұз кристалдарының нөлдік энтропиясын тәжірибе арқылы анықтаудан гөрі әлдеқайда дәлірек (ақауларды және энергия деңгейінің таралуын ескермей) есептеуге болады.
Ғалымдар және олардың осы саладағы жұмыстары
S 0=k B ˣ Ln (N E0) ретінде анықтауға болады, мұндағы k B - Больцман тұрақтысы, NE E энергиясындағы конфигурациялар саны, ал E0 - ең төменгі энергия. Кельвин нөліндегі алтыбұрышты мұз энтропиясының бұл мәні термодинамиканың үшінші заңын бұзбайды «Идеал кристалдың абсолютті нөлдегі энтропиясы дәл нөлге тең», өйткені бұл элементтер мен бөлшектер идеалды емес, сутектік байланысы ретсіз.
Бұл денеде сутегі байланысы кездейсоқ және тез өзгереді. Бұл құрылымдар энергия бойынша дәл бірдей емес, бірақ энергетикалық жақын күйлердің өте үлкен санына таралады, «мұз ережелеріне» бағынады. Нөлдік нүкте энтропиясы - бұл материалды абсолютті нөлге дейін салқындату мүмкін болса да (0 К=-273,15 ° C) болатын бұзылыс. Алтыбұрышты мұз 3, 41 (± 0, 2) ˣ моль -1 ˣ K -1 үшін тәжірибелік шатасуды тудырады. Теориялық тұрғыдан белгілі мұз кристалдарының нөлдік энтропиясын тәжірибе арқылы анықтаудан гөрі әлдеқайда дәлірек (ақауларды және энергия деңгейінің таралуын ескермей) есептеуге болады.

Үлкен мұздағы протондардың реті реттелген болмаса да, бет бұл бөлшектердің ілулі H-атомдарының жолақтары және O-жалғыз жұптары (реттелген сутегі байланыстары бар нөлдік энтропия) түріндегі тәртібін қалайды. ZPE нөлдік нүктенің бұзылуы, J ˣ моль -1 ˣ K -1 және т.б. Жоғарыда айтылғандардың барлығынан мұзға кристалдық торлардың қандай түрлері тән екені анық және түсінікті.






