Біз өмір сүріп жатқан әлем елестету мүмкін емес әдемі және өмір бағытын белгілейтін көптеген әртүрлі процестерге толы. Бұл процестердің барлығын белгілі ғылым - физика зерттейді. Ол кем дегенде ғаламның пайда болуы туралы түсінік алуға мүмкіндік береді. Бұл мақалада біз молекулалық-кинетикалық теория, оның теңдеулері, түрлері мен формулалары сияқты ұғымды қарастырамыз. Дегенмен, осы мәселелерді тереңірек зерттеуге көшпес бұрын, физиканың мәнін және оны зерттейтін салаларды нақтылап алуыңыз керек.
Физика дегеніміз не?

Шын мәнінде, бұл өте ауқымды ғылым және, мүмкін, адамзат тарихындағы ең іргелі ғылымдардың бірі. Мысалы, егер бірдей информатика адам іс-әрекетінің барлық дерлік саласымен байланысты болса, мейлі ол есептеу дизайны немесе мультфильмдер жасау болсын, онда физика өмірдің өзі, оның күрделі процестері мен ағындарының сипаттамасы болып табылады. Түсінуді мүмкіндігінше жеңілдете отырып, оның мағынасын ашуға тырысайық.
СоныменСонымен, физика - энергия мен материяны, олардың арасындағы байланыстарды, біздің ұлан-ғайыр ғаламда болып жатқан көптеген процестерді түсіндірумен айналысатын ғылым. Зат құрылымының молекулалық-кинетикалық теориясы физиканың теориялар мен салаларының теңізіндегі кішкене тамшы ғана.
Бұл ғылым егжей-тегжейлі зерттейтін энергияны әртүрлі формада көрсетуге болады. Мысалы, жарық, қозғалыс, ауырлық, радиация, электр тогы және басқа да көптеген нысандарда. Біз осы мақалада осы пішіндердің құрылымының молекулалық-кинетикалық теориясына тоқталамыз.
Материяны зерттеу бізге заттың атомдық құрылымы туралы түсінік береді. Айтпақшы, ол молекулалық-кинетикалық теориядан шығады. Материяның құрылымы туралы ғылым біздің болмысымыздың мәнін, өмірдің және Әлемнің пайда болу себептерін түсінуге және табуға мүмкіндік береді. Әлі де заттың молекулалық-кинетикалық теориясын зерттеуге тырысайық.
Біріншіден, терминологияны және кез келген қорытындыны толық түсіну үшін біраз кіріспе қажет.
Физика тақырыптары
Молекулалық-кинетикалық теория деген не деген сұраққа жауап бере отырып, физиканың бөлімдері туралы айтпай кетуге болмайды. Олардың әрқайсысы адам өмірінің белгілі бір саласын егжей-тегжейлі зерттеу және түсіндірумен айналысады. Олар келесідей жіктеледі:
- Механика, ол тағы екі бөлімге бөлінеді: кинематика және динамика.
- Статикалық.
- Термодинамика.
- Молекулалық бөлім.
- Электродинамика.
- Оптика.
- Кванттар физикасы және атом ядросы.
Молекулярлық туралы арнайы сөйлесейікфизика, себебі ол молекулалық-кинетикалық теорияға негізделген.
Термодинамика дегеніміз не?
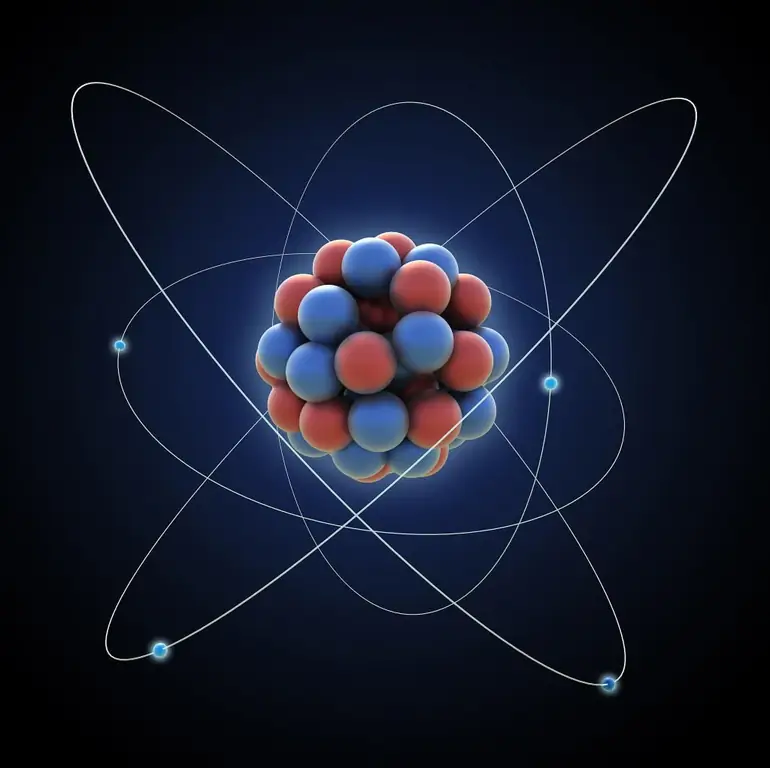
Жалпы, молекулалық бөлік пен термодинамика физикалық жүйелердің жалпы санының макроскопиялық құрамдас бөлігін ғана зерттейтін физиканың бір-бірімен тығыз байланысты салалары болып табылады. Бұл ғылымдар денелер мен заттардың ішкі күйін дәл сипаттайтынын есте ұстаған жөн. Мысалы, олардың қыздыру, кристалдану, булану және конденсация кезіндегі күйі, атомдық деңгейде. Басқаша айтқанда, молекулалық физика - бөлшектердің: атомдар мен молекулалардың орасан зор санынан тұратын жүйелер туралы ғылым.
Молекулярлық-кинетикалық теорияның негізгі ережелерін зерттеген осы ғылымдар болды.
Жетінші сыныптың өзінде микро және макроәлемдер, жүйелер ұғымдарымен таныстық. Бұл терминдерді жадта жаңарту артық болмайды.
Микроәлем, біз оның атауынан көріп отырғанымыздай, элементар бөлшектерден тұрады. Басқаша айтқанда, бұл ұсақ бөлшектер әлемі. Олардың өлшемдері 10-18 м мен 10-4 м диапазонында өлшенеді және олардың нақты күйінің уақыты шексіздікке де жетуі мүмкін. пропорционалды емес шағын интервалдар, мысалы, 10-20 s.
Macroworld көптеген элементар бөлшектерден тұратын тұрақты формалардың денелері мен жүйелерін қарастырады. Мұндай жүйелер адам өлшемімізге сәйкес келеді.
Сонымен қатар, мега әлем деген бар. Ол үлкен планеталардан, ғарыштық галактикалардан және кешендерден тұрады.
Негіздертеория
Енді біз аздап қайталап, физиканың негізгі терминдерін еске түсірдік, біз тікелей осы мақаланың негізгі тақырыбына өте аламыз.
Молекулалық-кинетикалық теория пайда болып, алғаш рет ХІХ ғасырда тұжырымдалған. Оның мәні Роберт Гук, Исаак сияқты көрнекті ғалымдардың болжамдарынан жинақталған үш іргелі ережеге сүйене отырып, кез келген заттың құрылымын (көбінесе қатты және сұйық денелерге қарағанда газдардың құрылымы) егжей-тегжейлі сипаттауында жатыр. Ньютон, Даниел Бернулли, Михаил Ломоносов және басқалар.
Молекулалық-кинетикалық теорияның негізгі ережелері келесідей естіледі:
- Мүлдем барлық заттар (сұйық, қатты немесе газ тәріздес болуына қарамастан) кішірек бөлшектерден: молекулалардан және атомдардан тұратын күрделі құрылымға ие. Атомдарды кейде "элементар молекулалар" деп те атайды.
- Бұл элементар бөлшектердің барлығы әрқашан үздіксіз және ретсіз қозғалыс күйінде болады. Біздің әрқайсымыз бұл ұсыныстың тікелей дәлеліне тап болдық, бірақ, ең алдымен, оған көп мән бермедік. Мысалы, күн сәулесінің фонында шаң бөлшектерінің үнемі ретсіз бағытта қозғалатынын бәріміз де көрдік. Бұл атомдар бір-біріне үнемі кинетикалық энергия беріп, өзара итермелейтіндігіне байланысты. Бұл құбылыс алғаш рет 1827 жылы зерттеліп, оны ашушының аты - «Браундық қозғалыс» деп атады.
- Барлық элементар бөлшектер бір-бірімен үздіксіз әрекеттесу процесіндеэлектрлік жынысы бар белгілі бір күштер.
Екінші позицияны сипаттайтын тағы бір мысал, мысалы, газдардың молекулалық-кинетикалық теориясына да қатысты болуы мүмкін диффузия екенін атап өткен жөн. Біз оны күнделікті өмірде және көптеген сынақтар мен бақылауларда кездестіреміз, сондықтан бұл туралы түсінік болуы маңызды.
Алдымен келесі мысалдарды қарастырыңыз:
Дәрігер абайсызда үстел үстіндегі колбадан алкогольді төгіп алды. Немесе сіз парфюмерия бөтелкеңізді түсіріп алсаңыз, ол бүкіл еденге тарап кеткен шығар.
Неліктен осы екі жағдайда алкогольдің иісі де, парфюмерияның иісі де осы заттардың ішіндегісі төгілген жерді ғана емес, біраз уақыттан кейін бүкіл бөлмені толтырады?
Жауап қарапайым: диффузия.
Диффузия - бұл не? Ол қалай ағып жатыр?

Бұл белгілі бір затты (әдетте газ) құрайтын бөлшектердің басқаның молекулааралық қуыстарына енетін процесс. Жоғарыда келтірілген мысалдарымызда келесі жағдай орын алды: термиялық, яғни үздіксіз және диссоциацияланған қозғалыстың әсерінен алкоголь және/немесе парфюмерия молекулалары ауа молекулалары арасындағы саңылауларға түсті. Бірте-бірте ауаның атомдарымен және молекулаларымен соқтығысудың әсерінен олар бөлменің айналасына таралады. Айтпақшы, диффузияның қарқындылығы, яғни оның ағынының жылдамдығы диффузияға қатысатын заттардың тығыздығына, сондай-ақ олардың атомдары мен молекулаларының кинетикалық деп аталатын қозғалыс энергиясына байланысты. Кинетикалық энергия неғұрлым көп болса, бұл молекулалардың жылдамдығы және қарқындылығы соғұрлым жоғары болады.
Ең жылдам диффузия процесін газдардағы диффузия деп атауға болады. Бұл газдың құрамы бойынша біртекті емес екеніне байланысты, яғни газдардағы молекулааралық бос орындар сәйкесінше айтарлықтай кеңістікті алады және оларға бөгде заттың атомдары мен молекулаларын алу процесі оңай және жылдамырақ жүреді..
Бұл процесс сұйықтықтарда сәл баяуырақ. Бір шыны шайда қант текшелерінің еруі қатты заттың сұйықтықтағы диффузиясының мысалы ғана.
Бірақ ең ұзақ уақыт - қатты кристалдық құрылымы бар денелердегі диффузия. Бұл дәл солай, өйткені қатты денелердің құрылымы біртекті және күшті кристалдық торға ие, оның жасушаларында қатты дененің атомдары тербеледі. Мысалы, екі металл сырықтың бетін жақсылап тазалап, содан кейін бір-бірімен жанасатын болса, онда жеткілікті ұзақ уақыт өткеннен кейін біз бір металдың басқа металдың бөліктерін анықтай аламыз және керісінше.
Кез келген басқа іргелі бөлімдер сияқты физиканың негізгі теориясы жеке бөліктерге бөлінеді: классификация, түрлер, формулалар, теңдеулер және т.б. Осылайша, біз молекулалық-кинетикалық теорияның негіздерін білдік. Бұл жеке теориялық блоктарды қарастыруға қауіпсіз өтуге болатынын білдіреді.
Газдардың молекулалық-кинетикалық теориясы
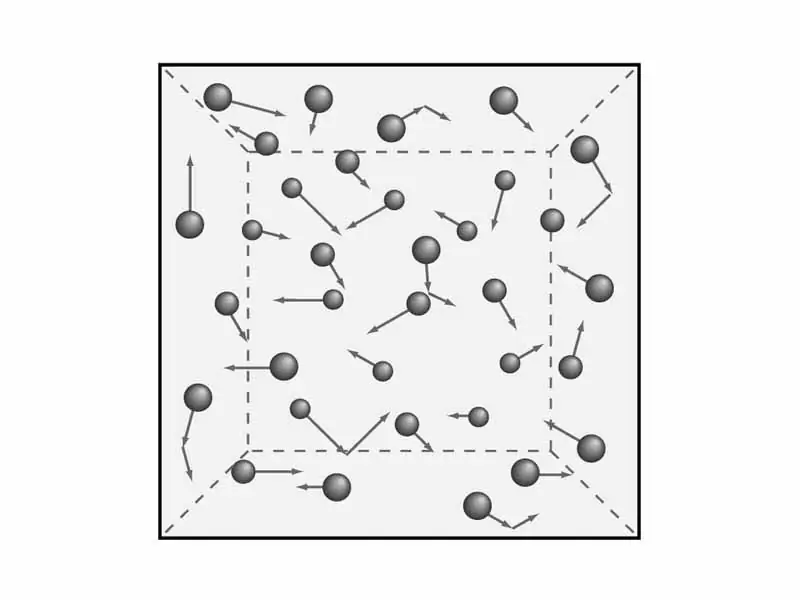
Газ теориясының ережелерін түсіну қажет. Жоғарыда айтқанымыздай, қысым мен температура сияқты газдардың макроскопиялық сипаттамаларын қарастырамыз. Бұлкейінірек газдардың молекулалық-кинетикалық теориясының теңдеуін шығару үшін қажет болады. Бірақ математика - кейінірек, ал енді теориямен және сәйкесінше физикамен айналысайық.
Ғалымдар газдардың кинетикалық моделін түсінуге қызмет ететін газдардың молекулалық теориясының бес ережесін тұжырымдады. Олар былай естіледі:
- Барлық газдар белгілі бір өлшемі жоқ, бірақ белгілі бір массасы бар элементар бөлшектерден тұрады. Басқаша айтқанда, бұл бөлшектердің көлемі олардың арасындағы ұзындықпен салыстырғанда ең аз.
- Газдардың атомдары мен молекулаларының іс жүзінде потенциалдық энергиясы жоқ, сәйкесінше заңға сәйкес барлық энергия кинетикалық энергияға тең.
- Бұл позициямен бұрынырақ танысқанбыз - броундық қозғалыс. Яғни, газ бөлшектері әрқашан үздіксіз және ретсіз қозғалыста болады.
- Жылдамдық пен энергия хабарымен жүретін газ бөлшектерінің барлық өзара соқтығысуы толығымен серпімді. Бұл соқтығыс кезінде олардың кинетикалық энергиясында энергия жоғалмайды немесе күрт секірулер болмайтынын білдіреді.
- Қалыпты жағдайда және тұрақты температурада барлық дерлік газдардың бөлшектер қозғалысының орташа энергиясы бірдей.
Газдардың молекулалық-кинетикалық теориясының теңдеуінің осы түрі арқылы біз бесінші орынды қайта жаза аламыз:
E=1/2mv^2=3/2kT, мұндағы k - Больцман тұрақтысы; T - Кельвиндегі температура.
Бұл теңдеу газдың элементар бөлшектерінің жылдамдығы мен олардың абсолютті температурасы арасындағы байланысты түсінуге мүмкіндік береді. Тиісінше, соғұрлым олардың абсолюттітемпература, олардың жылдамдығы мен кинетикалық энергиясы соғұрлым жоғары болады.
Газ қысымы
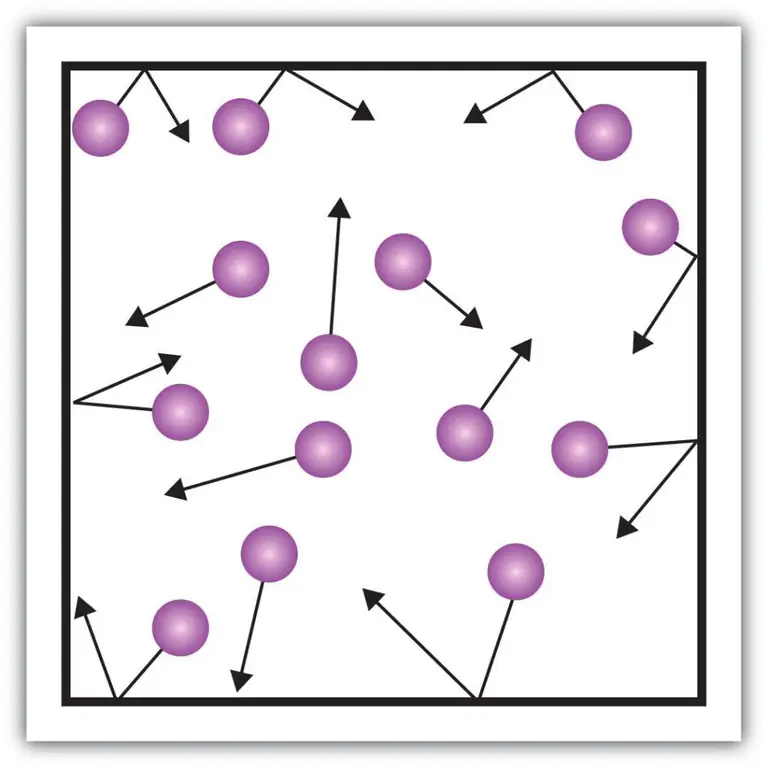
Сипаттаманың мұндай макроскопиялық құрамдас бөліктерін, мысалы, газдардың қысымын кинетикалық теория арқылы да түсіндіруге болады. Ол үшін келесі мысалды елестетіп көрейік.
Ұзындығы L болатын қорапта қандай да бір газдың молекуласы бар деп алайық. Жоғарыда сипатталған газ теориясының ережелерін қолданып, молекулалық сфера тек x бойымен қозғалатынын ескерейік. -ось. Осылайша, біз ыдыс (қорап) қабырғаларының бірімен серпімді соқтығысу процесін бақылай аламыз.
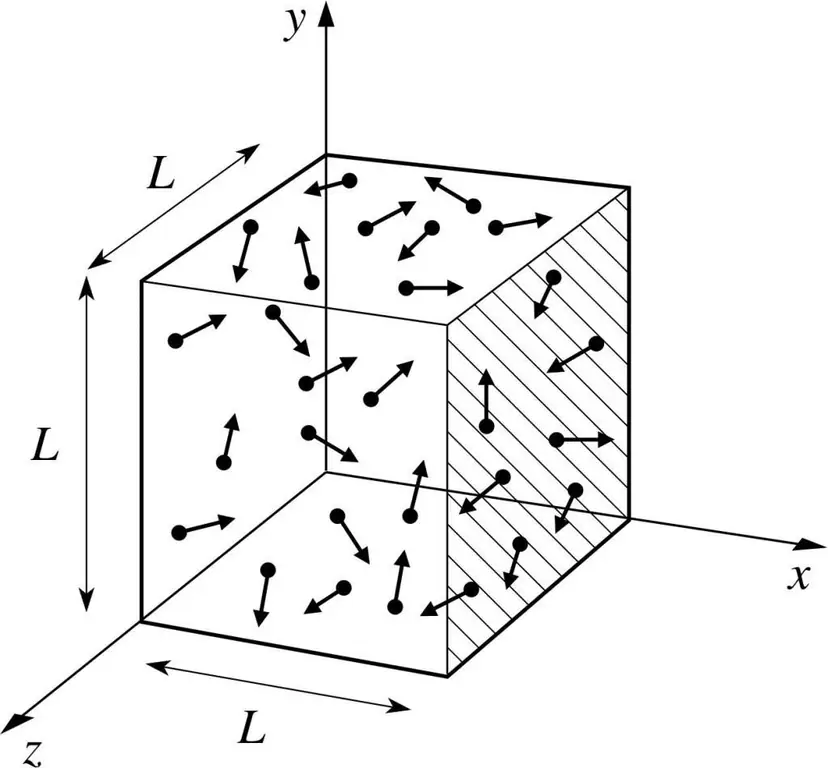
Ағымдағы соқтығыстың импульсі, біз білетіндей, мына формуламен анықталады: p=mv, бірақ бұл жағдайда бұл формула проекциялық пішінді қабылдайды: p=mv(x).
Біз тек x осінің өлшемін, яғни х осін қарастыратындықтан, импульстің жалпы өзгерісі мына формуламен өрнектелетін болады: mv(x) - m(-v() x))=2mv(x).
Содан кейін Ньютонның екінші заңын қолданып объектіміздің әсер ететін күшін қарастырайық: F=ma=P/t.
Бұл формулалардан газ жағынан қысымды өрнектейміз: P=F/a;
Енді алынған формулаға күш өрнегін қойып, мынаны аламыз: P=mv(x)^2/L^3.
Осыдан кейін біздің дайын қысым формуласын газ молекулаларының N-ші санына жазуға болады. Басқаша айтқанда, ол келесідей болады:
P=Nmv(x)^2/V, мұнда v - жылдамдық, V - дыбыс.
Енді газ қысымы туралы бірнеше негізгі ережелерді бөліп көрсетуге тырысайық:
- Ол арқылы көрінедімолекулалардың ол орналасқан нысанның қабырғаларының молекулаларымен соқтығысуы.
- Қысым шамасы молекулалардың ыдыс қабырғаларына әсер ету күші мен жылдамдығына тура пропорционал.
Теория бойынша кейбір қысқаша қорытындылар
Біз әрі қарай жүріп, молекулалық-кинетикалық теорияның негізгі теңдеуін қарастырмас бұрын, біз сізге жоғарыда аталған тармақтар мен теориядан бірнеше қысқаша қорытындыларды ұсынамыз:
- Оның атомдары мен молекулаларының орташа қозғалыс энергиясының өлшемі абсолютті температура болып табылады.
- Екі түрлі газ бірдей температурада болғанда, олардың молекулаларының орташа кинетикалық энергиясы бірдей болады.
- Газ бөлшектерінің энергиясы орташа квадраттық жылдамдыққа тура пропорционал: E=1/2mv^2.
- Газ молекулаларының сәйкесінше орташа кинетикалық энергиясы және орташа жылдамдығы болғанымен, жеке бөлшектер әртүрлі жылдамдықпен қозғалады: кейбіреулері жылдам, кейбіреулері баяу.
- Температура неғұрлым жоғары болса, молекулалардың жылдамдығы соғұрлым жоғары болады.
- Газдың температурасын қанша есе арттырсақ (мысалы, екі есе), оның бөлшектерінің қозғалыс энергиясы сонша есе артады (сәйкесінше екі есе өседі).
Негізгі теңдеу және формулалар

Молекулалық-кинетикалық теорияның негізгі теңдеуі микроәлемдегі шамалар мен сәйкесінше макроскопиялық, яғни өлшенген шамалар арасындағы байланысты орнатуға мүмкіндік береді.
Молекулалық теория қарастыратын қарапайым модельдердің бірі идеал газ үлгісі болып табылады.
Олай деуге боладыбұл идеал газдың молекулалық-кинетикалық теориясы зерттейтін ойдан шығарылған модельдің бір түрі, онда:
- ең қарапайым газ бөлшектері бір-бірімен де, кез келген ыдыс қабырғаларының молекулаларымен де әрекеттесетін тамаша серпімді шарлар ретінде қарастырылады, тек бір жағдайда - абсолютті серпімді соқтығыс;
- газдың ішіндегі тартылыс күштері жоқ немесе оларды елемеуге болады;
- материалдық нүктелер ретінде газдың ішкі құрылымының элементтерін алуға болады, яғни олардың көлемін де ескермеуге болады.
Осындай модельді қарастыра отырып, неміс физик Рудольф Клаузиус микро- және макроскопиялық параметрлердің байланысы арқылы газ қысымының формуласын жазды. Мынадай көрінеді:
p=1/3m(0)nv^2.
Кейінірек бұл формула идеал газдың молекулалық-кинетикалық теориясының негізгі теңдеуі деп аталады. Оны бірнеше түрлі формада көрсетуге болады. Біздің ендігі міндетіміз - молекулалық физика, молекула-кинетикалық теория сияқты бөлімдерді, демек олардың толық теңдеулері мен түрлерін көрсету. Сондықтан негізгі формуланың басқа нұсқаларын қарастырған жөн.
Газ молекулаларының қозғалысын сипаттайтын орташа энергияны мына формула арқылы табуға болатынын білеміз: E=m(0)v^2/2.
Бұл жағдайда бастапқы қысым формуласындағы m(0)v^2 өрнегін орташа кинетикалық энергиямен ауыстыра аламыз. Осының нәтижесінде газдардың молекулалық-кинетикалық теориясының негізгі теңдеуін келесі түрде құруға мүмкіндік аламыз: p=2/3nE.
Сонымен қатар, m(0)n өрнегін екі бөліктің көбейтіндісі түрінде жазуға болатынын бәріміз білеміз:
m/NN/V=m/V=ρ.
Осы манипуляциялардан кейін идеал газдың молекулалық-кинетикалық теориясының теңдеуінің формуласын үшінші, басқа түрде қайта жаза аламыз:
p=1/3ρv^2.
Осы тақырып бойынша білуіңіз керек нәрсе осы шығар. Алынған білімді қысқаша (олай емес) қорытындылар түрінде жүйелеу ғана қалады.
«Молекулалық-кинетикалық теория» тақырыбы бойынша барлық жалпы қорытындылар мен формулалар
Ендеше бастайық.
Бірінші:
Физика - зат пен энергияның қасиеттерін, олардың құрылысын, бейорганикалық табиғат заңдылықтарын зерттейтін жаратылыстану курсына кіретін іргелі ғылым.
Ол келесі бөлімдерді қамтиды:
- механика (кинематика және динамика);
- статикалық;
- термодинамика;
- электродинамика;
- молекулярлық бөлім;
- оптика;
- кванттар физикасы және атом ядросы.
Екінші:
Бөлшектер физикасы мен термодинамика - физикалық жүйелердің жалпы санының тек макроскопиялық құрамдас бөлігін, яғни элементар бөлшектердің орасан зор санынан тұратын жүйелерді зерттейтін бір-бірімен тығыз байланысты салалар.
Олар молекулалық-кинетикалық теорияға негізделген.
Үшінші:
Мәселенің түйіні мынада. Молекулярлық-кинетикалық теория заттың құрылымын егжей-тегжейлі сипаттайды (көбінесе қатты заттарға қарағанда газдардың құрылымы).және сұйық денелер), көрнекті ғалымдардың жорамалдарынан жиналған үш іргелі болжамға негізделген. Олардың ішінде: Роберт Гук, Исаак Ньютон, Дэниел Бернулли, Михаил Ломоносов және басқалар.
Төртінші:
Молекулалық-кинетикалық теорияның үш негізгі қағидасы:
- Барлық заттар (олардың сұйық, қатты немесе газ тәрізді болуына қарамастан) кішірек бөлшектерден: молекулалардан және атомдардан тұратын күрделі құрылымға ие.
- Бұл қарапайым бөлшектердің барлығы үздіксіз ретсіз қозғалыста. Мысалы: броундық қозғалыс және диффузия.
- Барлық молекулалар кез келген жағдайда бір-бірімен электрлік жынысы бар белгілі бір күштермен әрекеттеседі.
Молекулалық-кинетикалық теорияның осы ережелерінің әрқайсысы материяның құрылымын зерттеуде берік негіз болып табылады.
Бесінші:
Газ үлгісіне арналған молекулалық теорияның бірнеше негізгі тармақтары:
- Барлық газдар белгілі бір өлшемі жоқ, бірақ белгілі бір массасы бар элементар бөлшектерден тұрады. Басқаша айтқанда, бұл бөлшектердің көлемі олардың арасындағы қашықтықтармен салыстырғанда ең аз.
- Газдардың атомдары мен молекулаларының іс жүзінде потенциалдық энергиясы жоқ, сәйкесінше олардың жалпы энергиясы кинетикалық энергияға тең.
- Бұл позициямен бұрынырақ танысқанбыз - броундық қозғалыс. Яғни, газ бөлшектері әрқашан үздіксіз және кездейсоқ қозғалыста болады.
- Жылдамдық пен энергия хабарымен жүретін газдардың атомдары мен молекулаларының барлық өзара соқтығысуы толығымен серпімді болады. Бұлсоқтығыс кезінде олардың кинетикалық энергиясында энергия жоғалмайды немесе күрт секірулер болмайтынын білдіреді.
- Қалыпты жағдайда және тұрақты температурада барлық дерлік газдардың орташа кинетикалық энергиясы бірдей.
Алтыншы:
Газдар туралы теорияның қорытындылары:
- Абсолюттік температура - оның атомдары мен молекулаларының орташа кинетикалық энергиясының өлшемі.
- Екі түрлі газ бірдей температурада болғанда, олардың молекулаларының орташа кинетикалық энергиясы бірдей болады.
- Газ бөлшектерінің орташа кинетикалық энергиясы орташа квадраттық жылдамдыққа тура пропорционал: E=1/2mv^2.
- Газ молекулаларының сәйкесінше орташа кинетикалық энергиясы және орташа жылдамдығы болғанымен, жеке бөлшектер әртүрлі жылдамдықпен қозғалады: кейбіреулері жылдам, кейбіреулері баяу.
- Температура неғұрлым жоғары болса, молекулалардың жылдамдығы соғұрлым жоғары болады.
- Газдың температурасын қанша есе арттырсақ (мысалы, екі есе), оның бөлшектерінің орташа кинетикалық энергиясы да сонша есе артады (сәйкесінше, екі есе өседі).
- Газдың ол орналасқан ыдыстың қабырғаларындағы қысымы мен молекулалардың осы қабырғаларға әсер ету қарқындылығы арасындағы байланыс тура пропорционалды: соғұрлым көп соққы болса, соғұрлым қысым жоғары болады және керісінше.
Жетіншісі:
Идеал газ моделі келесі шарттар орындалуы керек үлгі болып табылады:
- Газ молекулалары мінсіз серпімді шарлар ретінде қарастырылады.
- Бұл шарлар бір-бірімен және кез келгеннің қабырғаларымен әрекеттесе аладыкеме тек бір жағдайда - абсолютті серпімді соқтығыс.
- Газ атомдары мен молекулалары арасындағы өзара итеруді сипаттайтын бұл күштер жоқ немесе оларды елемеуге болады.
- Атомдар мен молекулалар материалдық нүктелер ретінде қарастырылады, яғни олардың көлемін де ескермеуге болады.
Сегізінші:
«Молекулалық-кинетикалық теория» тақырыбындағы барлық негізгі теңдеулерді беріп, формулаларды көрсетейік:
p=1/3m(0)nv^2 - неміс физигі Рудольф Клаузиус шығарған идеал газ моделінің негізгі теңдеуі.
p=2/3nE - идеал газдың молекулалық-кинетикалық теориясының негізгі теңдеуі. Молекулалардың орташа кинетикалық энергиясынан алынған.
р=1/3ρv^2 - бірдей теңдеу, бірақ идеал газ молекулаларының тығыздығы мен орташа квадраттық жылдамдығы арқылы қарастырылады.
m(0)=M/N(a) - Авогадро саны арқылы бір молекуланың массасын табу формуласы.
v^2=(v(1)+v(2)+v(3)+…)/N - молекулалардың орташа квадраттық жылдамдығын табу формуласы, мұнда v(1), v(2), v (3) және т.б. - бірінші молекуланың жылдамдығы, екінші, үшінші және т.б. n-ші молекулаға дейін.
n=N/V - молекулалардың концентрациясын табу формуласы, мұндағы N - берілген V көлеміндегі газ көлеміндегі молекулалар саны.
E=mv^2/2=3/2kT - молекулалардың орташа кинетикалық энергиясын табуға арналған формулалар, мұнда v^2 - молекулалардың орташа квадраттық жылдамдығы, k - тұрақты Людвиг Больцманның физикасы Австрияның атымен аталған мән, ал T - газдың температурасы.
p=nkT - концентрация бойынша қысым формуласы, тұрақтыБольцман және абсолютті температура T. Одан орыс ғалымы Менделеев пен француз физик-инженері Клайперон ашқан тағы бір іргелі формула шығады:
pV=m/MRT, мұндағы R=kN(a) - газдар үшін әмбебап тұрақты.
Енді әртүрлі изопроцестер үшін тұрақтыларды көрсетейік: изобарлық, изохоралық, изотермиялық және адиабаттық.
pV/T=const - газдың массасы мен құрамы тұрақты болғанда орындалады.
рV=const - егер температура да тұрақты болса.
V/T=const - газ қысымы тұрақты болса.
p/T=const - дыбыс деңгейі тұрақты болса.
Мүмкін сізге осы тақырып бойынша білу керек нәрсе осы шығар.
Бүгін біз теориялық физика, оның көптеген бөлімдері мен блоктары сияқты ғылыми салаға еніп кеттік. Толығырақ, біз физиканың іргелі молекулалық физика және термодинамика сияқты саласын, атап айтқанда, бастапқы зерттеуде ешқандай қиындық тудырмайтын, бірақ шын мәнінде көптеген тұзақтары бар молекулалық-кинетикалық теорияны қозғадық.. Бұл идеалды газ моделі туралы түсінігімізді кеңейтеді, оны біз де егжей-тегжейлі зерттедік. Сонымен қатар, біз молекулалық теорияның негізгі теңдеулерімен олардың әртүрлі вариацияларымен таныстық, сонымен қатар осы тақырып бойынша белгілі бір белгісіз шамаларды табу үшін барлық қажетті формулаларды қарастырғанымызды атап өткен жөн. Бұл әсіресе жазуға дайындалған кезде пайдалы болады. кез келген сынақтар, емтихандар және сынақтар немесе физика туралы жалпы көзқарас пен білімді кеңейту.
Бұл мақала сізге пайдалы болды деп үміттенеміз және сіз одан молекулалық-кинетикалық теорияның негізгі ережелері сияқты термодинамика тіректеріндегі білімдеріңізді нығайта отырып, ең қажетті ақпаратты ғана алдыңыз.






