Біздің заманымызда физика өте кең таралған ғылымға айналды. Ол сөзбе-сөз барлық жерде бар. Ең қарапайым мысал: сіздің аулаңызда алма ағашы өсіп, оның үстінде жемістер піседі, уақыт келіп, алмалар түсе бастайды, бірақ олар қай бағытта түседі? Бүкіләлемдік тартылыс заңының арқасында біздің ұрық жерге түседі, яғни ол төмен түседі, бірақ жоғары емес. Бұл физиканың ең танымал мысалдарының бірі болды, бірақ термодинамикаға, дәлірек айтқанда, біздің өмірімізде маңыздылығы кем емес фазалық тепе-теңдікке назар аударайық.
Термодинамика

Алдымен осы терминге тоқталайық. ΘερΜοδυναΜική - бұл сөз грек тілінде осылай көрінеді. Бірінші бөлік ΘερΜo «жылу» дегенді білдіреді, ал екінші δυναΜική «күш» дегенді білдіреді. Термодинамика - макроскопиялық жүйенің қасиеттерін, сондай-ақ энергияны түрлендіру мен берудің әртүрлі тәсілдерін зерттейтін физиканың бір бөлімі. Бұл бөлімде температура түсінігін сипаттауға енгізу үшін әртүрлі күйлер мен процестер арнайы зерттеледі (бұл термодинамикалық жүйені сипаттайтын физикалық шама және оны пайдалану арқылы өлшенеді.белгілі бір құрылғылар). Термодинамикалық жүйелерде жүріп жатқан барлық процестер тек микроскопиялық шамалар (қысым мен температура, сонымен қатар компоненттердің концентрациясы) арқылы сипатталады.
Клапейрон-Клаузиус теңдеуі
Бұл теңдеуді әрбір физик біледі, бірақ оны бөлшектеп қарастырайық. Ол белгілі бір заттың бір фазадан екінші фазаға өтуінің тепе-теңдік процестерін білдіреді. Бұл мынандай мысалдарда анық көрінеді: балқыту, булану, сублимация (ылғалды толығымен жою арқылы өтетін өнімдерді сақтау тәсілдерінің бірі). Формула жүріп жатқан процестерді анық көрсетеді:
- n=PV/RT;
- мұндағы T - заттың температурасы;
- P-қысым;
- R-фазалық ауысудың меншікті жылуы;
- V-белгілі бір көлемдегі өзгеріс.
Теңдеудің жасалу тарихы

Клаузиус-Клапейрон теңдеуі термодинамиканың екінші заңының тамаша математикалық түсіндірмесі болып табылады. «Клаузиус теңсіздігі» деп те аталады. Әрине, теореманы жүйедегі жылу ағыны мен энтропия, сондай-ақ оны қоршаған орта арасындағы байланысты түсіндіргісі келген ғалымның өзі жасаған. Бұл теңдеуді Клаузиус энтропияны түсіндіру және сандық бағалау әрекеттерінде жасаған. Тура мағынада теорема бізге циклдік процестің қайтымды немесе қайтымсыз екенін анықтауға мүмкіндік береді. Бұл теңсіздік бізге екінші заңды түсінудің сандық формуласын ұсынады.
Ғалым энтропия идеясымен алғашқылардың бірі болып жұмыс істеді, тіпті оны берді.процесс атауы. Қазіргі уақытта Клаузиус теоремасы деп аталатын нәрсе алғаш рет 1862 жылы Рудольфтың «Интерьердегі жұмыс үшін трансформация эквиваленттік теоремасын пайдалану туралы» алтыншы жұмысында жарияланды. Ғалым жүйедегі қыздыру (δ Q) арқылы энтропия мен энергия ағыны арасындағы пропорционалды байланысты көрсетуге тырысты. Құрылыста бұл жылу энергиясын жұмысқа айналдыруға болады, ал ол циклдік процесс арқылы жылуға айналуы мүмкін. Рудольф «циклдік процесте болатын барлық түрлендірулердің алгебралық қосындысы тек нөлден аз немесе төтенше жағдайда нөлге тең болуы мүмкін»деп дәлелдеді.
Жабық оқшауланған жүйе
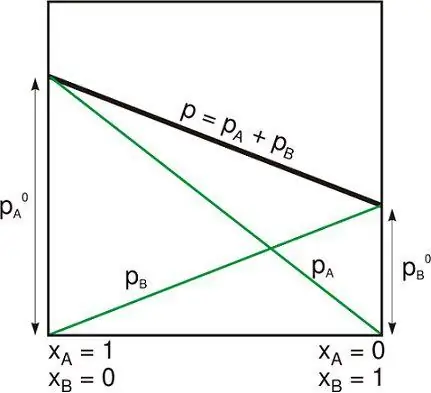
Оқшауланған жүйе мыналардың бірі:
- Физикалық жүйе олармен әрекеттеспейтін басқалардан алыс.
- Термодинамикалық жүйе зат та, энергия да өте алмайтын қатты қозғалмайтын қабырғалармен жабылған.
Субъект өзінің ауырлық күшімен іштей байланысты екеніне қарамастан, оқшауланған жүйе әдетте сыртқы гравитациялық және басқа да алыс күштердің шегінен тыс қабылданады.
Мұны (термодинамикада қолданылатын жалпы терминологияда) энергияны материя емес, жылу немесе жұмыс түрінде беруге болатын селективті қабырғалармен қоршалған жабық жүйе деп атауға болады. Материя мен энергия кіретін немесе шығатын ашық жүйемен, бірақ оның әртүрлі өтпейтін қабырғалары болуы мүмкін.оның шекараларының бөліктері.
Оқшауланған жүйе сақталу заңына бағынады. Көбінесе термодинамикада зат пен энергия жеке ұғымдар ретінде қарастырылады.
Термодинамикалық ауысулар
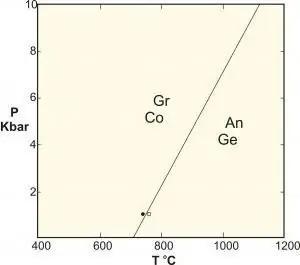
Кванттық фазалық ауысуларды түсіну үшін оларды классикалық түрлендірулермен (сонымен бірге жылулық инверсиялар деп те аталады) салыстыру пайдалы. CPT жүйенің термодинамикалық қасиеттерінің шыңын сипаттайды. Бұл бөлшектердің қайта құрылуын білдіреді. Типтік мысал - сұйық пен қатты дене арасындағы бірқалыпты өтуді сипаттайтын судың мұздату ауысуы. Классикалық фазалық өсулер жүйенің энергиясы мен оның жылулық тербелістерінің энтропиясы арасындағы бәсекеге байланысты.
Классикалық жүйеде нөлдік температурада энтропия болмайды, сондықтан фазалық түрлендіру болмайды. Олардың реті бірінші үзіліссіз туынды термодинамикалық потенциалмен анықталады. Және, әрине, оның бірінші тәртібі бар. Ферромагнетиктен парамагнетикке фазалық түрлендірулер үздіксіз және екінші ретті. Бұл реттелген фазадан ретсіз фазаға тұрақты өзгерістер нөлге тең реттілік параметрімен сипатталады. Жоғарыда аталған ферромагниттік түрлендіру үшін реттік параметр жүйенің жалпы магниттелуі болады.
Гиббс потенциалы
Гиббстің бос энергиясы - термодинамикалық жабық жүйеден (жылу алмасуға және қоршаған ортамен жұмыс істеуге) алынуы мүмкін кеңеюсіз жұмыстың максималды көлемі. Мұндаймаксималды нәтиже толығымен қайтымды процесте ғана алынуы мүмкін. Жүйе бірінші күйден екінші күйге қайта оралғанда, Гиббс бос энергиясының азаюы қысым күштерінің жұмысын алып тастағандағы жүйенің өз ортасында орындағанына тең болады.
Баланс күйлері

Термодинамикалық және механикалық тепе-теңдік термодинамиканың аксиоматикалық түсінігі. Бұл көп немесе аз өткізгіш немесе өткізбейтін қабырғалармен қосылған бір немесе бірнеше жүйелердің ішкі күйі. Бұл күйде жүйе ішінде де, жүйелер арасында да заттардың немесе энергияның таза макроскопиялық ағындары болмайды.
Ішкі тепе-теңдік күйінің өзіндік тұжырымдамасында макроскопиялық өзгеріс болмайды. Жүйелер бір мезгілде өзара жылулық, механикалық, химиялық (тұрақты), радиациялық тепе-теңдікте болады. Олар бірдей пішінде болуы мүмкін. Бұл процесте физикалық операция бұзылғанша барлық көріністер бірден және шексіз сақталады. Макроскопиялық тепе-теңдікте өте дәл теңдестірілген алмасулар орын алады. Жоғарыдағы дәлел бұл ұғымның физикалық түсіндірмесі болып табылады.
Негіздер
Әр заңдардың, теоремалардың, формулалардың өз негіздері бар. Фазалық тепе-теңдік заңының 3 негізін қарастырайық.
- Фаза - заттың химиялық құрамы, физикалық жағдайы және механикалық тепе-теңдігі бойынша біртекті түрі. Типтік фазалар қатты, сұйық және газ тәрізді. Жеке шекарамен бөлінген екі араласпайтын сұйықтықтар (немесе құрамы әртүрлі сұйық қоспалар) екі бөлек фаза және араласпайтын қатты заттар болып саналады.
- Компоненттер саны (C) - жүйенің химиялық тәуелсіз компоненттерінің саны. Жүйенің барлық фазаларының құрамын анықтау үшін қажетті тәуелсіз түрлердің ең аз саны.
- Бұл контексттегі еркіндік дәрежелерінің саны (F) бір-бірінен тәуелсіз қарқынды айнымалылар саны болып табылады.
Фазалық тепе-теңдік бойынша жіктеу
- Үздіксіз таза тасымалдау реакциялары (көбінесе қатты күйдегі реакциялар деп аталады) құрамы әртүрлі қатты заттар арасында жүреді. Олар сұйықтарда кездесетін элементтерді қамтуы мүмкін (H, C), бірақ бұл элементтер қатты фазаларда сақталады, сондықтан реакцияға түсетін заттар немесе өнімдер ретінде сұйық фазалар қатыспайды (H2O, CO2). Қатты таза тасымалдау реакциялары үздіксіз немесе үзіліссіз немесе терминалды болуы мүмкін.
- Полиморфты - құрамы бірдей фазаларды қамтитын қатты фазалық реакцияның ерекше түрі. Классикалық мысалдар алюминий силикаттары кианит-силлиманит-андалузит арасындағы реакциялар, жоғары қысымда графиттің алмазға айналуы және кальций карбонатының тепе-теңдігі болып табылады.
Тепе-теңдік заңдары

Гиббс зауытының ережесін Джозия Уиллард Гиббс 1875 жылдан 1878 жылға дейін шыққан «Гетерогенді заттардың тепе-теңдігі» атты әйгілі мақаласында ұсынған. Ол қолданыладытермодинамикалық тепе-теңдіктегі реактивті емес көпкомпонентті гетерогенді жүйелер және берілген теңдік:
- F=C-P+2;
- мұндағы F - еркіндік дәрежелерінің саны;
- C - компоненттер саны;
- P - бір-бірімен термодинамикалық тепе-теңдіктегі фазалар саны.
Еркіндік дәрежелерінің саны бос қарқынды айнымалылар саны. Бір мезгілде және бір-біріне әсер етпестен ерікті түрде өзгеруі мүмкін температура немесе қысым сияқты термодинамикалық параметрлердің ең үлкен саны. Бір компонентті жүйенің мысалы ретінде бір таза химиялық зат бар жүйені келтіруге болады, ал су мен этанол қоспалары сияқты екі компонентті жүйелерде екі тәуелсіз компонент бар. Әдеттегі фазалық ауысулар (фазалық тепе-теңдік) қатты заттар, сұйықтар, газдар болып табылады.
Тұрақты қысымдағы фаза ережесі
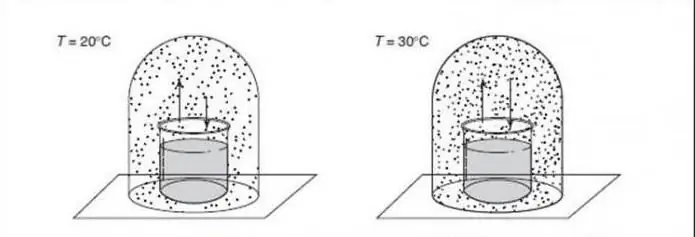
Әртүрлі қатты құрылымдар арасындағы фазалық өзгерістермен айналысатын материалтану қолданбалары үшін тұрақты қысым жиі пайда болады (мысалы, бір атмосфера) және еркіндік дәрежесі ретінде еленбейді, сондықтан ереже келесідей болады: F=C - P + 1.
Бұл формула кейде «конденсацияланған фаза ережесі» деген атпен енгізіледі, бірақ біз білетіндей, бұл жоғары қысымға ұшырайтын жүйелерге (мысалы, геологияда) қолданылмайды, өйткені олардың салдары қысым апатты салдарға әкелуі мүмкін.
Фазалық тепе-теңдік бос сөз болып көрінуі мүмкін және осы сәтте болатын физикалық процестер аз.қатысады, бірақ, байқағанымыздай, онсыз біз білетін көптеген заңдар жұмыс істемейді, сондықтан сіз осы ерекше, түрлі-түсті, аз болса да қызықсыз ережелермен аздап танысуыңыз керек. Бұл білім көптеген адамдарға көмектесті. Оларды өздеріне қолдануды үйренді, мысалы, электриктер фазалармен жұмыс істеу ережелерін біле отырып, өздерін қажетсіз қауіптен қорғай алады.






