Идеал газдың қасиеттерін зерттеу физикадағы маңызды тақырып болып табылады. Газ жүйелерінің сипаттамаларымен таныстыру Бойль-Мариотт теңдеуін қарастырудан басталады, өйткені ол идеал газдың эксперименталды түрде ашылған бірінші заңы болып табылады. Оны мақалада толығырақ қарастырайық.
Идеал газ дегеніміз не?
Бойл-Мариотт заңы және оны сипаттайтын теңдеу туралы айтпас бұрын, идеал газды анықтайық. Ол әдетте оны құрайтын бөлшектер бір-бірімен әрекеттеспейтін сұйық зат ретінде түсініледі және олардың өлшемдері орташа бөлшектер аралық қашықтықтармен салыстырғанда елеусіздей кішкентай.
Шындығында кез келген газ нақты, яғни оның құрамдас атомдары мен молекулалары белгілі бір өлшемге ие және ван-дер-Ваальс күштерінің көмегімен бір-бірімен әсерлеспейді. Бірақ жоғары абсолютті температурада (300 К-ден жоғары) және төмен қысымда (бір атмосферадан аз) атомдар мен молекулалардың кинетикалық энергиясы ван-дер-Ваальс әрекеттесу энергиясынан әлдеқайда жоғары, сондықтан нақты газ көрсетілген кезде.жоғары дәлдіктегі шарттарды идеалды деп санауға болады.
Бойл-Мариотт теңдеуі
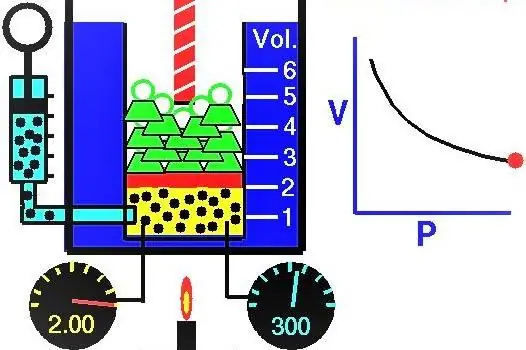
Газдардың қасиеттері Еуропа ғалымдары XVII-XIX ғасырларда белсенді түрде зерттеді. Тәжірибе жүзінде ашылған ең бірінші газ заңы газ жүйесінің кеңеюі мен қысылуының изотермиялық процестерін сипаттайтын заң болды. Сәйкес эксперименттерді 1662 жылы Роберт Бойл және 1676 жылы Эдм Мариотт жүргізді. Бұл ғалымдардың әрқайсысы тұйық газ жүйесіндегі изотермиялық процесс кезінде қысымның көлемге кері өзгеретінін өз бетінше көрсетті. Процестің тәжірибелік жолмен алынған математикалық өрнегі келесі түрде жазылады:
PV=k
Мұнда P және V жүйедегі қысым және оның көлемі, k - кейбір тұрақты, оның мәні газ затының мөлшері мен оның температурасына байланысты. P(V) функциясының графикке тәуелділігін құрсаңыз, онда ол гипербола болады. Бұл қисықтардың мысалы төменде көрсетілген.
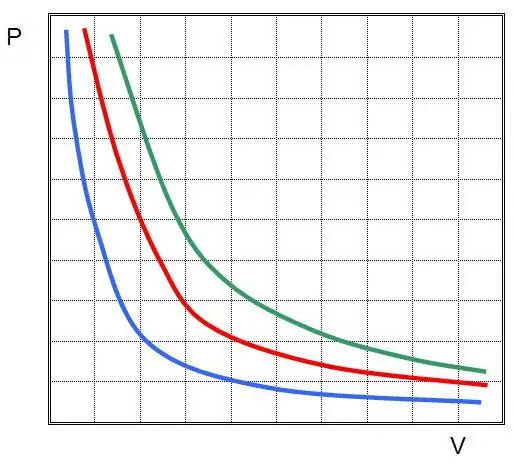
Жазбаша теңдік Бойль-Мариот теңдеуі (заңы) деп аталады. Бұл заңды қысқаша былайша тұжырымдауға болады: тұрақты температурада идеал газдың кеңеюі ондағы қысымның пропорционалды төмендеуіне әкеледі, керісінше, газ жүйесінің изотермиялық сығуы ондағы қысымның пропорционалды жоғарылауымен бірге жүреді.
Идеал газ теңдеуі
Бойл-Мариотт заңы Менделеев және аттарымен аталатын неғұрлым жалпы заңның ерекше жағдайы болып табылады. Клапейрон. Эмиль Клапейрон 1834 жылы әртүрлі сыртқы жағдайларда газдардың әрекеті туралы тәжірибелік ақпаратты қорытындылай отырып, келесі теңдеуді алды:
PV=nRT
Басқаша айтқанда, газ жүйесінің V көлемі мен ондағы P қысымының көбейтіндісі абсолютті температура T және n зат мөлшерінің көбейтіндісіне тура пропорционал. Бұл пропорционалдық коэффициенті R әрпімен белгіленеді және газ әмбебап тұрақтысы деп аталады. Жазбаша теңдеуде R мәні 1874 жылы Дмитрий Иванович Менделеев жасаған бірқатар тұрақтыларды ауыстыру есебінен пайда болды.
Әмбебап күй теңдеуінен температура мен зат мөлшерінің тұрақтылығы теңдеудің оң жағының өзгермейтіндігіне кепілдік беретінін байқау қиын емес, яғни теңдеудің сол жағы да тұрақты болып қалады.. Бұл жағдайда Бойль-Мариотт теңдеуін аламыз.

Басқа газ заңдары
Жоғарыдағы абзацта жазылған Клапейрон-Менделеев теңдеуінде үш термодинамикалық параметр бар: P, V және T. Егер олардың әрқайсысы бекітілген болса, ал қалған екеуінің өзгеруіне рұқсат етілсе, онда Бойль-Мариотты аламыз, Чарльз және Гей-Люссак теңдеулері. Чарльз заңы изобарлық процесс үшін көлем мен температура арасындағы тура пропорционалдылық туралы айтады, ал Гей-Люссак заңы изохоралық ауысу жағдайында газ қысымы абсолютті температураға тура пропорционалды өседі немесе төмендейді. Сәйкес теңдеулер келесідей:
V/T=const кезінде P=const;
P/T=const кезде V=const.
СоныменСонымен, Бойль-Мариотт заңы үш негізгі газ заңдарының бірі болып табылады. Бірақ оның басқаларынан графикалық тәуелділігі бойынша ерекшеленеді: V(T) және P(T) функциялары түзу сызықтар, P(V) функциясы гипербола.
Бойл-Мариотт заңын қолдануға арналған тапсырманың мысалы
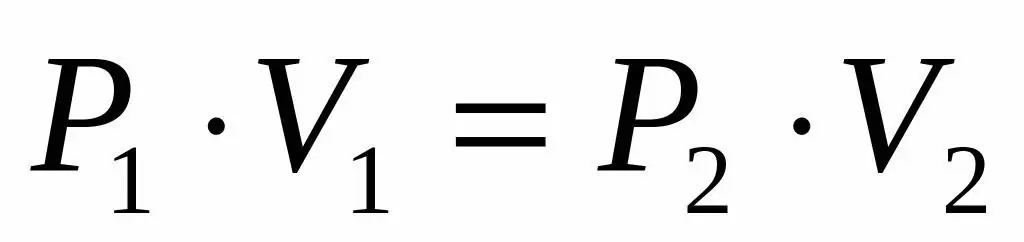
Бастапқы қалпында поршень астындағы цилиндрдегі газдың көлемі 2 литр, ал қысымы 1 атмосфера болды. Поршень көтеріліп, газ жүйесінің көлемі 0,5 литрге артқаннан кейін газдың қысымы қандай болды. Процесс изотермиялық болып саналады.
Бізге идеал газдың қысымы мен көлемі берілгендіктен, сондай-ақ оның кеңеюі кезінде температураның өзгермейтінін білетіндіктен, Бойль-Мариотт теңдеуін келесі түрде қолдануға болады:
P1V1=P2V 2
Бұл теңдік берілген температурадағы газдың әрбір күйі үшін көлем-қысым өнімі тұрақты екенін айтады. Теңдіктен P2 мәнін өрнектеп, соңғы формуланы аламыз:
P2=P1V1/V 2
Қысым есептеулерін жасаған кезде, бұл жағдайда жүйеден тыс қондырғыларды пайдалануға болады, өйткені литрлер азаяды және біз атмосферада P2 қысымын аламыз. Шарттың деректерін ауыстыра отырып, мәселенің сұрағына жауап аламыз: P2=0,8 атмосфера.






