Газдың жылу сыйымдылығы деп денені бір градусқа қыздырғанда сіңіретін энергияны айтады. Осы физикалық шаманың негізгі сипаттамаларын талдап көрейік.

Анықтамалар
Газдың меншікті жылуы - белгілі бір заттың бірлік массасы. Оның өлшем бірліктері Дж/(кг·К). Ағзаның агрегаттық күйін өзгерту процесінде сіңіретін жылу мөлшері тек бастапқы және соңғы күймен ғана емес, сонымен қатар ауысу әдісімен де байланысты.

Бөлім
Газдардың жылу сыйымдылығы тұрақты көлемде (Cv), тұрақты қысымда (Cр) анықталған шамаға бөлінеді.
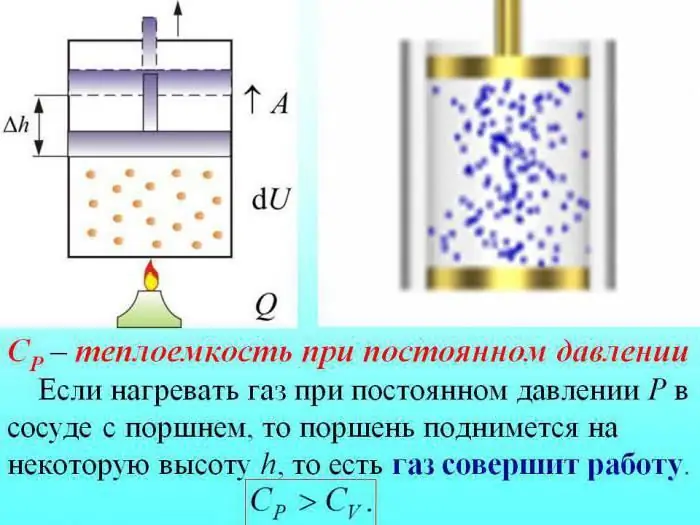
Қысымды өзгертпей қыздыру жағдайында газдың кеңею жұмысын өндіруге жылудың біраз бөлігі жұмсалады, ал энергияның бір бөлігі ішкі энергияны арттыруға жұмсалады.
Тұрақты қысымдағы газдардың жылу сыйымдылығы ішкі энергияны арттыруға жұмсалатын жылу мөлшерімен анықталады.
Газ күйі: мүмкіндіктері, сипаттамасы
Идеал газдың жылу сыйымдылығы Сp-Сv=R екенін ескере отырып анықталады. Соңғы шама әмбебап газ тұрақтысы деп аталады. Оның мәні 8,314 Дж/(моль К) сәйкес келеді.
Жылу сыйымдылығының теориялық есептеулерін жүргізгенде, мысалы, температурамен байланысын сипаттағанда, тек термодинамикалық әдістерді қолдану жеткіліксіз, статикалық физика элементтерімен қарулану маңызды.
Газдардың жылу сыйымдылығы кейбір молекулалардың ілгерілемелі қозғалысы энергиясының орташа мәнін есептеуді қамтиды. Мұндай қозғалыс молекуланың айналмалы және ілгерілемелі қозғалыстарынан, сондай-ақ атомдардың ішкі тербелістерінен қорытындыланады.
Статикалық физикада айналмалы және ілгерілемелі қозғалыс еркіндігінің әрбір дәрежесі үшін әмбебап газ тұрақтысының жартысына тең газ мөлшері болатыны туралы ақпарат бар.

Қызықты фактілер
Бір атомды газдың бөлшегі үш ілгерілемелі еркіндік дәрежесіне ие деп есептеледі, сондықтан газдың меншікті жылуы үш ілгерілемелі, екі айналу және бір діріл еркіндік дәрежесіне ие. Олардың біркелкі таралу заңы тұрақты көлемдегі меншікті жылуды R-ге теңестіруге әкеледі.
Тәжірибе барысында екі атомды газдың жылусыйымдылығы R шамасына сәйкес келетіні анықталды. Теория мен практиканың мұндай сәйкессіздігі идеал газдың жылу сыйымдылығы кванттықпен байланысты екендігімен түсіндіріледі. әсерлері, сондықтан есептеулерді жасаған кезде кванттық статистиканы пайдалану маңыздымеханика.
Кванттық механика негіздеріне сүйене отырып, тербелетін немесе айналатын кез келген бөлшектер жүйесі, соның ішінде газ молекулалары энергияның кейбір дискретті мәндеріне ғана ие болады.
Егер жүйедегі жылулық қозғалыс энергиясы белгілі бір жиіліктегі тербелістерді қоздыру үшін жеткіліксіз болса, мұндай қозғалыстар жүйенің жалпы жылу сыйымдылығына ықпал етпейді.
Нәтижесінде белгілі бір еркіндік дәрежесі «қатып қалады», оған тең бөлу заңын қолдану мүмкін емес.
Газдардың жылу сыйымдылығы бүкіл термодинамикалық жүйенің жұмыс істеуі тәуелді болатын күйдің маңызды сипаттамасы болып табылады.
Дірілдеу немесе айналу еркіндік дәрежесіне тең бөлу заңын қолдануға болатын температура кванттық теориямен сипатталады, Планк тұрақтысын Больцман тұрақтысымен байланыстырады.

Диатомды газдар
Мұндай газдардың айналу энергиясы деңгейлерінің арасындағы алшақтықтар аз дәрежелі. Ерекшелік - температура мәні жүздеген градуспен анықталатын сутегі.
Сондықтан тұрақты қысымдағы газдың жылу сыйымдылығын біркелкі таралу заңымен сипаттау қиын. Кванттық статистикада жылу сыйымдылығын анықтау кезінде оның тербеліс бөлігі температура төмендеген жағдайда тез азайып, нөлге жететіні ескеріледі.
Бұл құбылыс бөлме температурасында жылу сыйымдылығының тербеліс бөлігінің іс жүзінде жоқ екендігін түсіндіреді,екі атомды газ, ол R тұрақтысына сәйкес келеді.
Төмен температуралық индикаторлар жағдайында тұрақты көлемдегі газдың жылу сыйымдылығы кванттық статистика көмегімен анықталады. Термодинамиканың үшінші бастамасы деп аталатын Нернст принципі бар. Оның формуласына сүйене отырып, газдың молярлық жылу сыйымдылығы температураның төмендеуімен нөлге дейін төмендейді.

Қатты заттардың ерекшеліктері
Егер газдар қоспасының жылу сыйымдылығын кванттық статистика арқылы түсіндіруге болатын болса, онда агрегаттың қатты күйі үшін жылулық қозғалыс тепе-теңдік жағдайына жақын бөлшектердің шамалы ауытқуымен сипатталады.
Әр атомның үш тербеліс еркіндік дәрежесі бар, сондықтан тең бөлу заңына сәйкес қатты дененің молярлық жылу сыйымдылығын 3nR деп есептеуге болады, бұл ретте n молекуладағы атомдар саны болады.
Тәжірибеде бұл сан қатты дененің жылу сыйымдылығы жоғары температураға ұмтылатын шек болып табылады.
Кейбір элементтер, соның ішінде металдар үшін кәдімгі температурада максималды алуға болады. n=1 үшін Дюлонг және Пети заңы орындалады, бірақ күрделі заттар үшін мұндай шекке жету өте қиын. Шындығында шекті алу мүмкін болмағандықтан, қатты заттың ыдырауы немесе балқуы орын алады.
Кванттық теорияның тарихы
Кванттық теорияның негізін салушылар - ХХ ғасырдың басындағы Эйнштейн мен Дебай. Ол белгілі бір шамада атомдардың тербелмелі қозғалыстарын кванттауға негізделгенкристал. Төмен температура көрсеткіштері жағдайында қатты дененің жылу сыйымдылығы текшеленген абсолютті шамаға тура пропорционал болып шығады. Бұл қатынас Дебай заңы деп аталды. Төмен және жоғары температура көрсеткіштерін ажыратуға мүмкіндік беретін критерий ретінде олардың Дебай температурасымен салыстыруы алынады.
Бұл мән денедегі атомның тербеліс спектрімен анықталады, сондықтан оның кристалдық құрылымының ерекшеліктеріне айтарлықтай тәуелді.
QD - бірнеше жүз K бар мән, бірақ, мысалы, алмазда ол әлдеқайда жоғары.
Өткізгіш электрондар металдардың жылу сыйымдылығына үлкен үлес қосады. Оны есептеу үшін Ферми кванттық статистикасы қолданылады. Металл атомдары үшін электрондық өткізгіштік абсолютті температураға тура пропорционал. Ол шамалы мән болғандықтан, ол абсолютті нөлге бейім температураларда ғана ескеріледі.
Жылу сыйымдылығын анықтау әдістері
Негізгі эксперименттік әдіс - калориметрия. Жылу сыйымдылығының теориялық есебін жүргізу үшін статистикалық термодинамика қолданылады. Ол идеал газ үшін де, кристалдық денелер үшін де жарамды, материяның құрылымы туралы тәжірибелік деректер негізінде жүзеге асырылады.
Идеал газдың жылу сыйымдылығын есептеудің эмпирикалық әдістері химиялық құрылым идеясына, атомдардың жеке топтарының Ср үлесіне негізделген.
Сұйықтар үшін термодинамикалық қолдануға негізделген әдістер де қолданыладыбулану процесінің энтальпиясының температурасының туындысы арқылы идеал газдың жылу сыйымдылығынан сұйыққа өтуге мүмкіндік беретін циклдар.
Ерітінді жағдайында жылу сыйымдылығын аддитивтік функция ретінде есептеуге жол берілмейді, өйткені ерітіндінің жылу сыйымдылығының артық мәні негізінен маңызды.
Оны бағалау үшін ерітінділердің молекулалық-статистикалық теориясы қажет. Ең қиыны термодинамикалық талдауда гетерогенді жүйелердің жылу сыйымдылығын анықтау.

Қорытынды
Жылу сыйымдылығын зерттеу химиялық реакторларда, сондай-ақ басқа химиялық өндіріс аппараттарында болатын процестердің энергетикалық балансын есептеуге мүмкіндік береді. Сонымен қатар, бұл мән салқындату сұйықтарының оңтайлы түрлерін таңдау үшін қажет.
Қазіргі уақытта заттардың термодинамикалық сипаттамаларын анықтаудың негізгі нұсқасы әртүрлі температуралық интервалдар үшін - төмен мәндерден жоғары мәндерге дейін заттардың жылу сыйымдылығын эксперименталды түрде анықтау болып табылады. Заттың энтропиясы мен энтальпиясын есептеу кезінде жылу сыйымдылық интегралдар қолданылады. Белгілі бір температура диапазонындағы химиялық реагенттердің жылу сыйымдылығы туралы ақпарат процестің жылу эффектісін есептеуге мүмкіндік береді. Ерітінділердің жылу сыйымдылығы туралы ақпарат олардың термодинамикалық параметрлерін талданатын аралықтағы кез келген температура мәндерінде есептеуге мүмкіндік береді.
Мысалы, сұйықтық потенциалдық энергияның мәнін өзгерту үшін жылудың бір бөлігін жұмсауымен сипатталады.реакцияға түсетін молекулалар. Бұл мән шешімдерді сипаттау үшін пайдаланылатын "конфигурация" жылу сыйымдылығы деп аталады.
Заттың термодинамикалық сипаттамаларын, оның агрегаттық күйін есепке алмай, толыққанды математикалық есептеулер жүргізу қиын. Сондықтан сұйықтықтар, газдар, қатты заттар үшін заттың энергетикалық параметрлерін сипаттауға мүмкіндік беретін меншікті жылу сыйымдылығы сияқты сипаттама қолданылады.






