Физикада газдардың әрекетін зерттегенде изопроцестерге, яғни бір термодинамикалық параметр сақталатын жүйе күйлері арасындағы мұндай ауысуларға көп көңіл бөлінеді. Бірақ күйлер арасында газдық ауысу бар, ол изопроцесс емес, табиғат пен технологияда маңызды рөл атқарады. Бұл адиабаталық процесс. Бұл мақалада біз оны толығырақ қарастырып, газдың адиабаталық көрсеткішінің не екеніне назар аударамыз.
Адиабаталық процесс
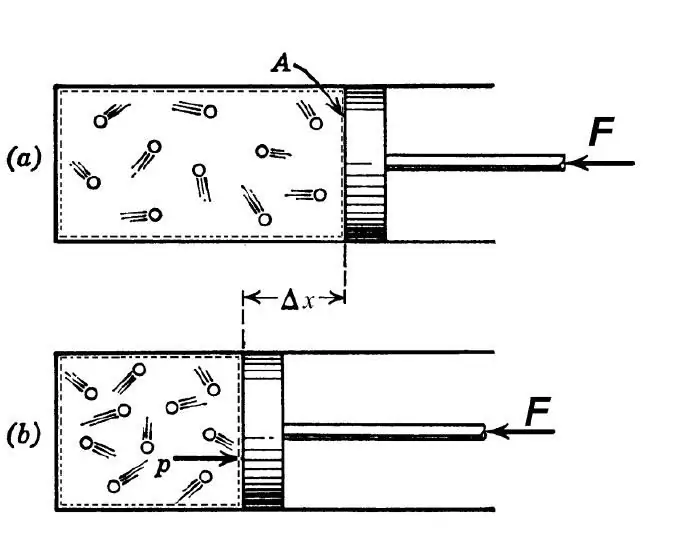
Термодинамикалық анықтамаға сәйкес адиабаталық процесс деп жүйенің бастапқы және соңғы күйлері арасындағы осындай ауысу түсініледі, нәтижесінде сыртқы орта мен зерттелетін жүйе арасында жылу алмасу болмайды. Мұндай процесс келесі екі жағдайда мүмкін болады:
- сыртқы орта мен арасындағы жылуөткізгіштікжүйе бір немесе басқа себептермен төмен;
- процесс жылдамдығы жоғары, сондықтан жылу алмасудың орын алуына уақыты жоқ.
Техникада адиабаталық ауысу газды күрт сығу кезінде қыздыру үшін де, жылдам кеңею кезінде оны салқындату үшін де қолданылады. Табиғатта қарастырылып отырған термодинамикалық ауысу ауа массасы төбеден көтерілгенде немесе төмен түскенде көрінеді. Мұндай көтерілулер ауадағы шық нүктесінің және жауын-шашынның өзгеруіне әкеледі.
Адиабаталық идеал газ үшін Пуассон теңдеуі

Идеал газ деп бөлшектері жоғары жылдамдықпен кездейсоқ қозғалатын, бір-бірімен әрекеттеспейтін және өлшемсіз болатын жүйені айтады. Мұндай модель математикалық сипаттамасы жағынан өте қарапайым.
Адиабаталық процестің анықтамасы бойынша термодинамиканың бірінші заңына сәйкес келесі өрнекті жазуға болады:
dU=-PdV.
Басқаша айтқанда, кеңейетін немесе жиырылатын газ өзінің ішкі энергиясының dU сәйкес өзгеруіне байланысты PdV жұмыс істейді.
Идеал газ жағдайында күй теңдеуін қолдансақ (Клапейрон-Менделеев заңы), келесі өрнекті алуға болады:
PVγ=тұрақты.
Бұл теңдік Пуассон теңдеуі деп аталады. Газ физикасымен таныс адамдар, егер γ мәні 1-ге тең болса, онда Пуассон теңдеуі Бойль-Мариотт заңына (изотермиялық) енетінін байқайды.процесс). Дегенмен, теңдеулерді мұндай түрлендіру мүмкін емес, өйткені идеал газдың кез келген түрі үшін γ бірден үлкен. γ (гамма) шамасы идеал газдың адиабаталық көрсеткіші деп аталады. Оның физикалық мағынасын толығырақ қарастырайық.
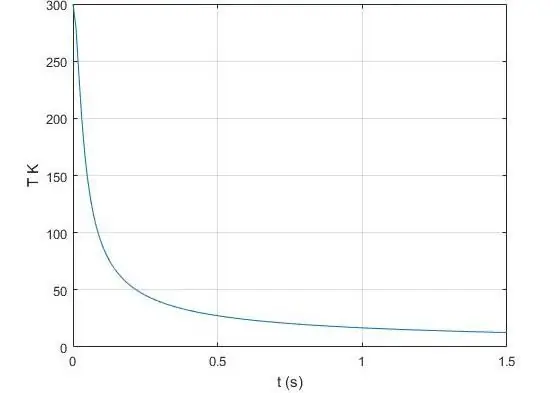
Адиабаталық көрсеткіш дегеніміз не?
Идеал газ үшін Пуассон теңдеуінде пайда болатын γ көрсеткіші тұрақты қысымдағы жылу сыйымдылығының бірдей мәнге қатынасы, бірақ қазірдің өзінде тұрақты көлемде. Физикада жылу сыйымдылығы - бұл оның температурасын 1 Кельвинге өзгерту үшін берілген жүйеге берілуі немесе алынуы керек жылу мөлшері. Изобарлық жылу сыйымдылықты CP символымен, ал изохоралық жылу сыйымдылықты CV белгісімен белгілейміз. Сонда теңдік γ үшін орындалады:
γ=CP/CV.
γ әрқашан бірден үлкен болғандықтан, ол зерттелетін газ жүйесінің изобарлық жылу сыйымдылығы ұқсас изохоралық сипаттамадан қанша есе артық екенін көрсетеді.
CP және CV жылу сыйымдылығы
Адиабаталық көрсеткішті анықтау үшін CP және CV шамаларының мағынасын жақсы түсіну керек. Ол үшін келесі ой тәжірибесін жүргіземіз: газдың қабырғалары тұтас ыдыста тұйық жүйеде екенін елестетіңіз. Егер ыдыс қыздырылса, онда барлық берілген жылу газдың ішкі энергиясына айналады. Мұндай жағдайда теңдік жарамды болады:
dU=CVdT.
МәнCV жүйені 1 К-ге изохоралық қыздыру үшін оны беру керек жылу мөлшерін анықтайды.
Енді газ қозғалатын поршені бар ыдыста болсын делік. Мұндай жүйені жылыту процесінде поршень тұрақты қысымның сақталуын қамтамасыз ете отырып, қозғалады. Бұл жағдайда жүйенің энтальпиясы изобарлық жылусыйымдылық пен температураның өзгеруінің көбейтіндісіне тең болатындықтан, термодинамиканың бірінші бастамасы келесі формада болады:
CPdT=CVdT + PdV.
Осы жерден CP>CV екенін көруге болады, өйткені күйлердің изобарлық өзгеруі жағдайында жылуды жүйенің температурасын, демек оның ішкі энергиясын ғана емес, сонымен бірге оның кеңеюі кезіндегі газдың жұмысын да жоғарылатуға жұмсаңыз.
Идеал бір атомды газ үшін γ мәні
Ең қарапайым газ жүйесі - бір атомды идеал газ. Бізде осындай газдың 1 мольі бар делік. Еске салайық, 1 моль газды бар болғаны 1 Кельвинге изобарлық қыздыру процесінде ол R-ге тең жұмыс істейді. Бұл таңба әдетте әмбебап газ тұрақтысын белгілеу үшін қолданылады. Ол 8, 314 Дж / (мольК) тең. Осы жағдай үшін алдыңғы абзацтағы соңғы өрнекті қолданып, біз келесі теңдікті аламыз:
CP=CV+ R.
Одан изохоралық жылусыйымдылықтың мәнін анықтауға болады CV:
γ=CP/CV;
CV=R/(γ-1).
Бір моль үшін екені белгілібір атомды газ, изохоралық жылу сыйымдылығының мәні:
CV=3/2R.
Соңғы екі теңдіктен адиабаталық көрсеткіштің мәні шығады:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
γ мәні тек газдың өзінің ішкі қасиеттеріне (молекулаларының көп атомдылығына) байланысты екенін және жүйедегі заттың мөлшеріне тәуелді емес екенін ескеріңіз.
γ-тің еркіндік дәрежесінің санына тәуелділігі
Бір атомды газдың изохоралық жылусыйымдылығының теңдеуі жоғарыда жазылған. Онда пайда болған 3/2 коэффициенті бір атомдағы еркіндік дәрежелерінің санына байланысты. Оның кеңістіктің үш бағытының біреуінде ғана қозғалу мүмкіндігі бар, яғни еркіндіктің аудармалық дәрежелері ғана бар.
Егер жүйе екі атомды молекулалардан құралса, үш трансляциялық деңгейге тағы екі айналу дәрежесі қосылады. Демек, CV өрнегі келесіге айналады:
CV=5/2R.
Онда γ мәні болады:
γ=7/5=1, 4.
Екі атомды молекуланың шын мәнінде тағы бір еркіндік дәрежесі бар екенін ескеріңіз, бірақ бірнеше жүз Кельвин температурасында ол белсендірілмейді және жылу сыйымдылығына ықпал етпейді.
Егер газ молекулалары екі атомнан көп болса, онда олардың 6 еркіндік дәрежесі болады. Бұл жағдайда адиабаталық көрсеткіш келесіге тең болады:
γ=4/3 ≈ 1, 33.
СоныменОсылайша, газ молекуласындағы атомдар саны көбейген сайын γ мәні азаяды. Егер сіз P-V осьтерінде адиабаталық графикті салсаңыз, бір атомды газ үшін қисық полиатомдыға қарағанда күртірек болатынын байқайсыз.
Газдар қоспасы үшін адиабаталық көрсеткіш
Біз жоғарыда γ мәні газ жүйесінің химиялық құрамына тәуелді емес екенін көрсеттік. Дегенмен, бұл оның молекулаларын құрайтын атомдар санына байланысты. Жүйе N құрамдас бөліктен тұрады деп алайық. Қоспадағы i компонентінің атомдық үлесі ai. Содан кейін қоспаның адиабаталық көрсеткішін анықтау үшін келесі өрнекті қолдануға болады:
γ=∑i=1N(aiγ i).
Мұндағы γi - i-ші құрамдас үшін γ мәні.
Мысалы, бұл өрнек ауаның γ мәнін анықтау үшін пайдаланылуы мүмкін. Ол оттегі мен азоттың 99% екі атомды молекулаларынан тұратындықтан, оның адиабаталық индексі 1,4 мәніне өте жақын болуы керек, бұл осы мәнді эксперименттік анықтаумен расталады.






